江苏集萃药康生物科技股份有限公司品牌商
7 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
江苏集萃药康生物科技股份有限公司
入驻年限:7 年
- 联系人:
药康生物
- 所在地区:
江苏 南京市 浦口区
- 业务范围:
抗体、细胞库 / 细胞培养、技术服务、试剂、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 代理商 科研机构
公司新闻/正文
肿瘤免疫经典研究荟萃:NCG小鼠助力解码肿瘤免疫新机制
26 人阅读发布时间:2026-04-20 09:49
免疫缺陷小鼠,特别是重度免疫缺陷小鼠模型在生物医药研究中具有重要作用,由于其T细胞、B细胞和NK细胞功能重度缺失,为外源细胞或组织移植提供了理想的体内环境。近年来,伴随肿瘤免疫学、干细胞研究及基因编辑等领域的进展,重度免疫缺陷小鼠模型已被广泛用于人类肿瘤异种移植、人源化免疫系统重建以及免疫疗法药效评价等方面。借助这类模型,研究人员能够在活体层面更真实地模拟人类疾病的进展与治疗反应,从而推动基础研究成果向临床应用的快速转化。
KLHL6蛋白通过调控蛋白质稳态抵抗T细胞耗竭【Nature,2026】
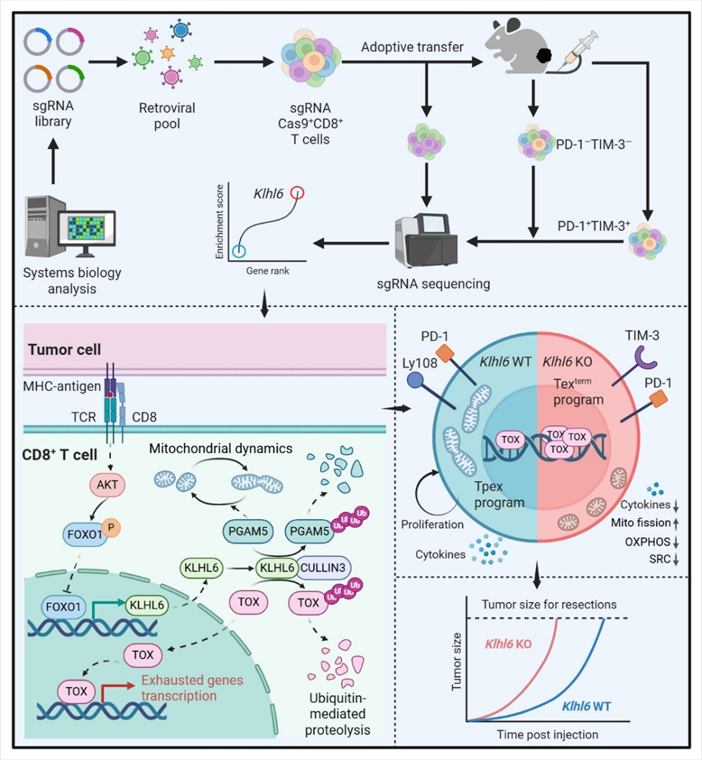
图1. KLH6调控机制
2026年1月,中国医学科学院系统医学研究院/苏州系统医学研究所李贵登团队与Fred Hutchinson癌症研究中心的Philip D. Greenberg团队合作,在《Nature》上发表题为“The Ubiquitin Ligase KLHL6 Drives Resistance to CD8(+) T Cell Dysfunction”的研究论文。研究揭示:持续 TCR 信号通过抑制 FOXO1 转录活性,导致 E3 泛素连接酶 KLHL6 持续性下调,这一关键分子事件是驱动 CD8⁺ T 细胞走向耗竭的核心 “开关”。KLHL6的降低抑制了耗竭核心调控因子TOX以及线粒体稳态因子PGAM5的降解,从而启动耗竭程序并破坏线粒体功能,最终推动T细胞向终末耗竭状态分化并失去抗肿瘤能力。此项突破从蛋白信号转导与蛋白稳态调控的全新维度,系统解答了 “持续抗原刺激如何驱动 T 细胞耗竭” 的重大科学问题,为肿瘤免疫机制研究提供了里程碑式的理论依据[1]。
药康生物NCG小鼠(品系编号:T001475)为该重大发现提供了关键临床前模型支撑,成功推动癌症免疫治疗领域创新。研究团队利用NCG构建了人源化肝癌移植瘤模型,有效验证了KLHL6可显著提升TCR-T细胞在肿瘤微环境中的浸润、存活及功能持久性,为突破肿瘤免疫治疗瓶颈提供了新的靶点和临床前评价工具。
NCG-Gfi1−/−人源免疫系统重建模型揭示特定分化阶段的中性粒细胞特性【Cell Research,2025】
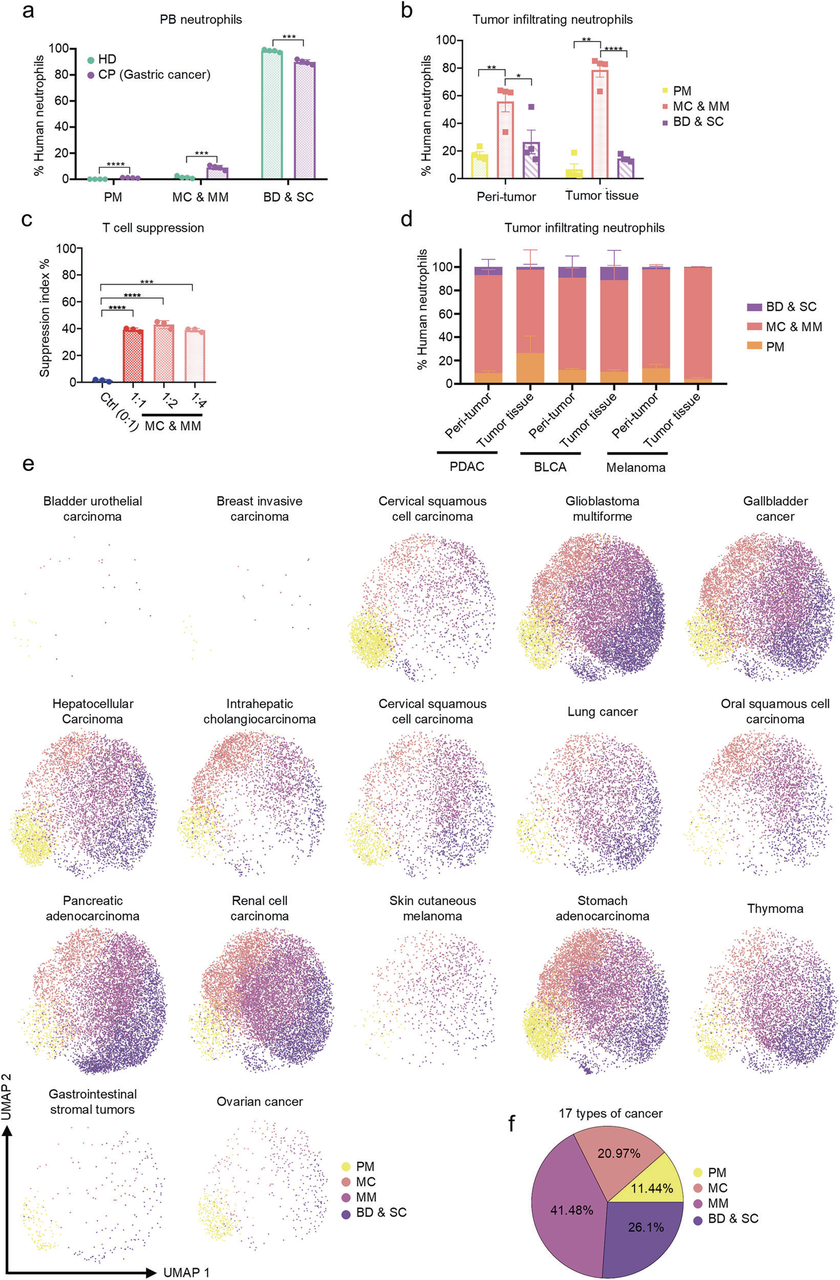
图2. MC & MM 中性粒细胞构成不同肿瘤类型中的 TINs 主体
2025年7月,南京大学模式动物研究所李颜教授团队、南京大学医学院附属鼓楼医院肿瘤中心魏嘉教授团队、康奈尔大学医学院Taha Merghoub教授团队,以及新乡医学院医学技术学院梁银明教授团队,在《Cell Research》上合作发表了题为“Human myelocyte and metamyelocyte-stage neutrophils suppress tumor immunity and promote cancer progression”的研究论文。该研究首次揭示,人类骨髓来源的中幼粒及晚幼粒阶段中性粒细胞具备显著免疫抑制功能与促肿瘤进展作用,且该关键表型在小鼠模型中未被观测到,揭示了人与小鼠在肿瘤免疫调控机制上的重要物种差异[2]。
研究团队以重度免疫缺陷NCG小鼠为基础,通过敲除调控中性粒细胞发育的关键转录因子Gfi1,并移植人源肿瘤浸润中性粒细胞(TINs),成功构建了人源化免疫重建小鼠模型(NCG-Gfi1−/−HIS)。该模型精准重现了肿瘤患者骨髓中髓细胞(MC)与后髓细胞(MM)占主导的特征,并在肿瘤浸润中性粒细胞中得到了验证。通过对骨髓中性粒细胞进行单细胞RNA测序分析,研究者进一步发现CD63与Galectin-3可作为区分上述两类细胞的关键表面标志物。此外,研究提出了一种潜在治疗策略:利用Fms样酪氨酸激酶3配体(Flt3L)诱导中晚幼阶段中性粒细胞向单核细胞分化。在NCG‑Gfi1−/−HIS 人源化模型中验证显示,该策略可显著抑制肿瘤生长并实现有效肿瘤控制。
肝细胞癌代谢免疫调控新靶点——eIF3f【Journal of Hepatology,2025】
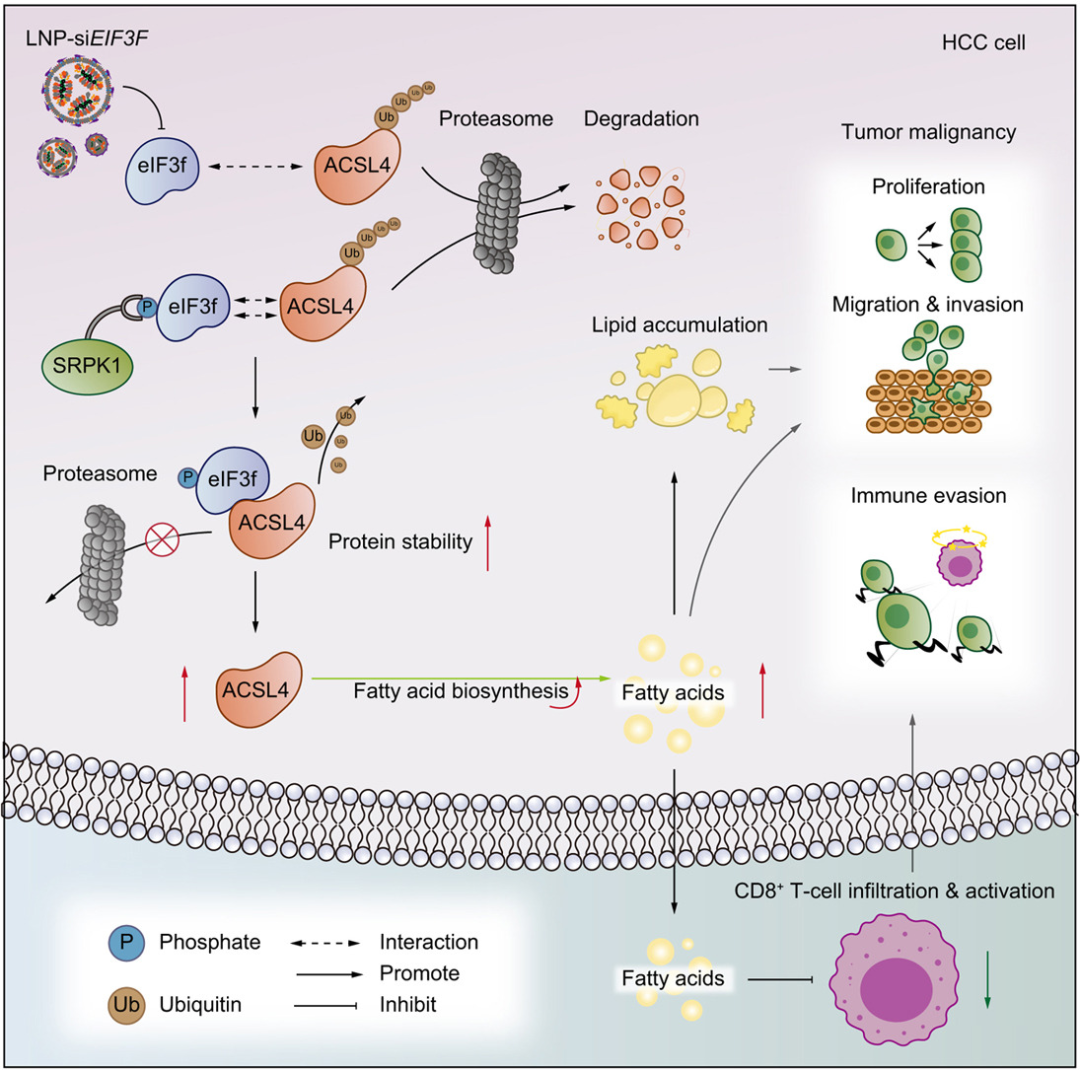
图3. eIF3f相关分子机制
本研究用NCG小鼠等多种免疫缺陷小鼠以及肝癌类器官,系统开展体内外功能验证,结果显示,在免疫缺陷的活体环境中,敲低eIF3f能有效抑制肿瘤生长、脂质积累及远处转移,而过表达eIF3f则产生相反的促癌效果。多模型结果相互印证,有效排除小鼠宿主因素干扰,直接、有力地证明了eIF3f本身具有驱动HCC恶性进展的独立致癌能力,为其分子机制提供了关键的体内实验证据。
基于血清外泌体ncRNA的胃癌早期诊断模型【Gut,2025】
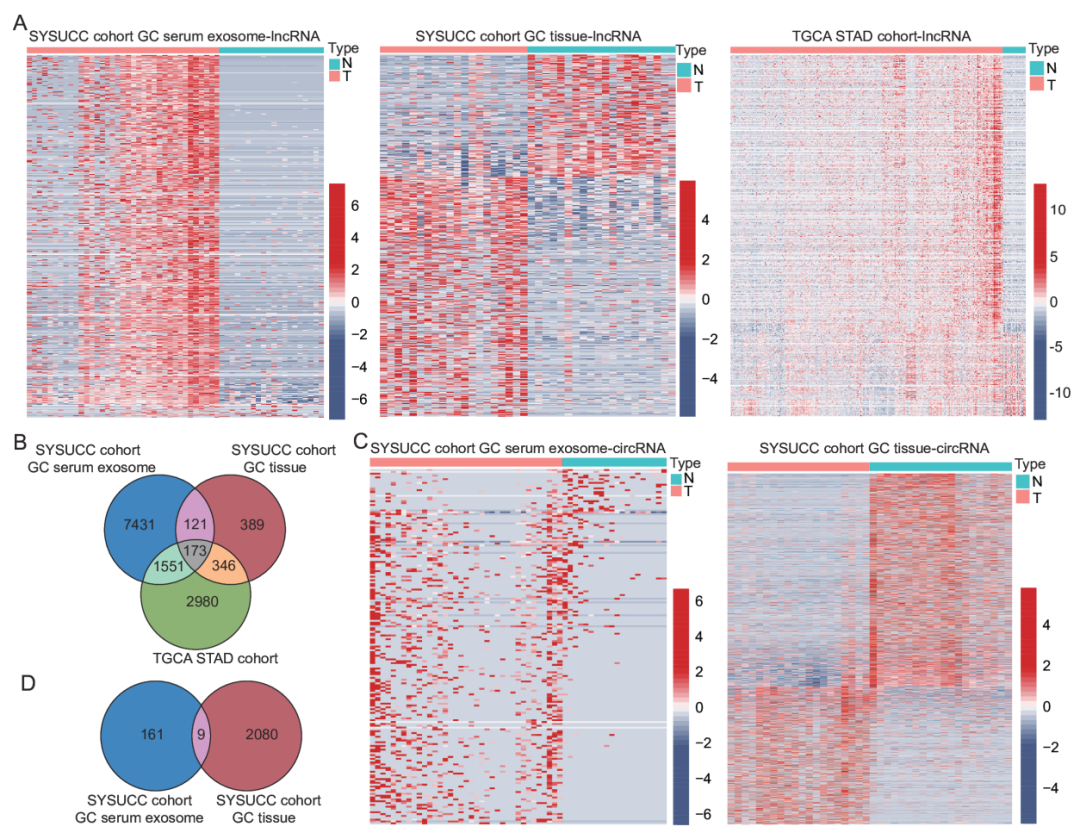
图4. 外泌体来源的非编码RNA的筛选
2025年1月3日,来自中山大学肿瘤防治中心的鞠怀强教授团队在《Gut》杂志发表题为“Construction of exosome non-coding RNA feature for non-invasive, early detection of gastric cancer patients by machine learning: a multi-cohort study”的一项多队列研究,旨在通过机器学习鉴定胃癌早期的血清外泌体非编码RNA特征以提升胃癌诊断能力。研究通过RNA测序筛选182个候选标志物,在518例胃癌患者与460名健康对照中验证31个潜在标志物。基于四个长链非编码RNA(RP11.443C10.1、CTD-2339L15.3、LINC00567、DGCR9)的联合诊断评分,在训练集、测试集及外部验证集中均表现出优异的区分效能,且诊断性能优于传统肿瘤标志物;可有效识别传统标志物阴性胃癌及早期胃癌病例[4]。
尽管该研究以临床样本与计算建模为核心,在外泌体标志物的筛选、验证及功能机制研究的转化阶段,仍依赖小鼠模型开展关键体内验证。研究使用NCG小鼠移植胃癌细胞系(CDX)或患者来源组织(PDX)构建肿瘤模型,评估外泌体标志物的动态变化与诊断窗口,并通过体内功能实验验证DGCR9等靶点对肿瘤生长的调控作用。NCG 小鼠为上述外泌体诊断标志物及功能靶点提供了稳定可靠的体内评价平台,有力推动胃癌无创诊断策略从基础研究向临床前转化迈进。
以上研究展示了重度免疫缺陷小鼠NCG小鼠在肿瘤免疫与精准诊断中的核心价值。从分子机制解析、关键靶点鉴定到新型治疗策略验证,基于 NCG 小鼠构建的人源化免疫重建模型及CDX/PDX 异种移植模型,有效弥补了物种差异带来的局限,可在活体水平高度模拟人源肿瘤微环境与免疫应答特征,为肿瘤靶点的精准筛选、功能验证及临床前转化提供了不可或缺的关键平台。
NCG 小鼠(T001475) 是药康生物自主知识产权的重度免疫缺陷模型,以T、B、NK 三重缺陷实现高成活率人源移植与人源化免疫系统重建,广泛用于肿瘤 CDX/PDX、免疫治疗评价、精准药效筛选,为肿瘤免疫与转化医学提供核心体内验证平台。
参考文献
[1] Nature . 2026 Mar;651(8105):451-461.
[2] Cell Res . 2025 Aug;35(8):588-606.
[3] J Hepatol . 2025 Sep;83(3):712-728.
[4] Gut . 2025 May 7;74(6):884-893.






