江苏集萃药康生物科技股份有限公司品牌商
7 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
文献支持
B6-IL10 KO 小鼠模型 疾病模型 基因敲除小鼠
¥605
品牌商
江苏集萃药康生物科技股份有限公司
入驻年限:7 年
- 联系人:
药康生物
- 所在地区:
江苏 南京市 浦口区
- 业务范围:
抗体、细胞库 / 细胞培养、技术服务、试剂、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 代理商 科研机构
公司新闻/正文
神秘而复杂的消化道疾病—炎症性肠病(IBD)
2962 人阅读发布时间:2022-08-04 17:57
炎症性肠病(Inflammatory Bowel DiseaseIBD)是一种新兴疾病,最初于19世纪工业革命时期在西方国家被报道1,随着人类社会工业化和生活方式西式化的转变,IBD的发病率逐年上升,到目前全球已有超过1000万人罹患此病。

图1 在世界IBD日被紫色灯光照射的世界各地

图2 世界IBD日的“紫丝带”标志
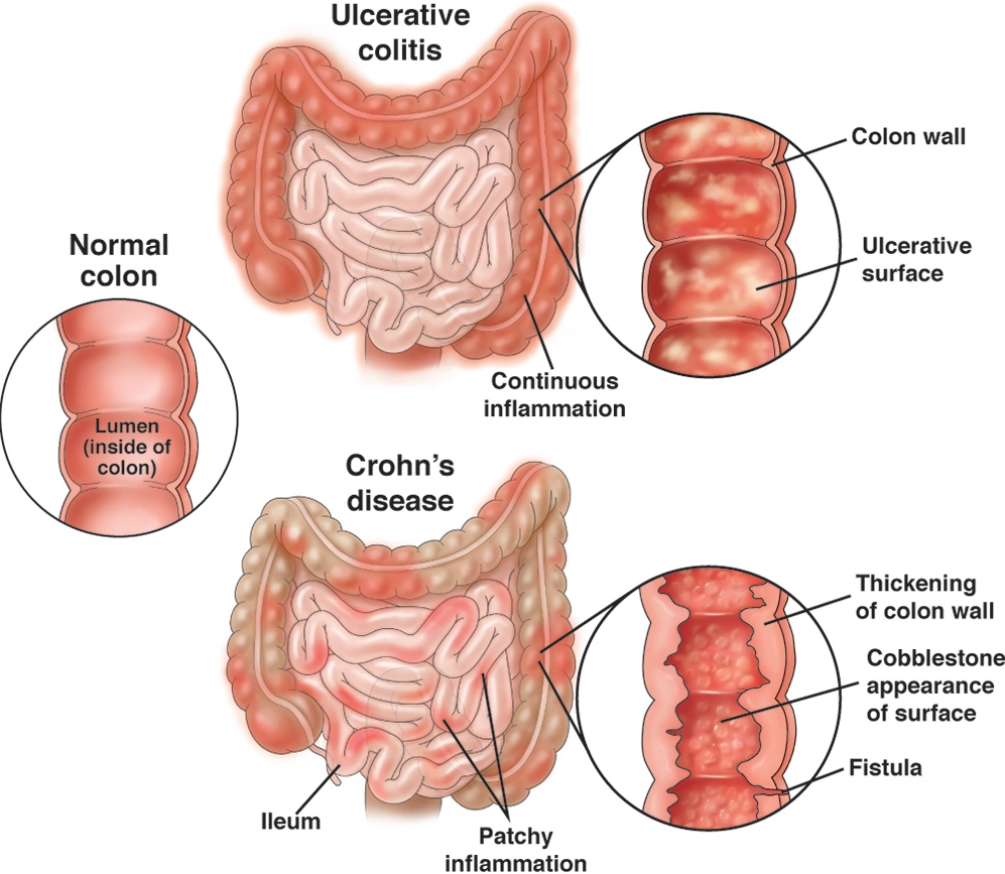
图3 UC和CD的肠道表现
在基因层面,目前已经发现约250个基因位点与IBD有关,包括与上皮屏障、免疫反应、细胞自噬、细胞凋亡、氧化应激相关的基因[6]。这说明在IBD发病机制中存在基因与免疫系统以及肠道上皮之间的复杂关联。
在免疫层面,IBD的慢性炎症反应与免疫系统的调节失衡和过度激活存在直接联系(图4)。一般认为,免疫系统的激活起始于结肠上皮的破损和外界抗原的入侵,最初会引起固有免疫的激活,树突细胞、巨噬细胞、嗜中性粒细胞等会参与到这个过程中。而随着免疫系统和消化道炎症的反复激活,最终将逐渐形成不可逆的慢性炎症,这主要与适应免疫的激活有关。其中,Th1和Th17细胞及其相关炎性因子的激活被认为与CD发病有关;而Th2和Th17细胞及其相关炎性因子的激活被认为与UC发病有关。此外,调节T细胞、固有淋巴细胞、B细胞等也参与到了IBD的免疫进程中[7]。
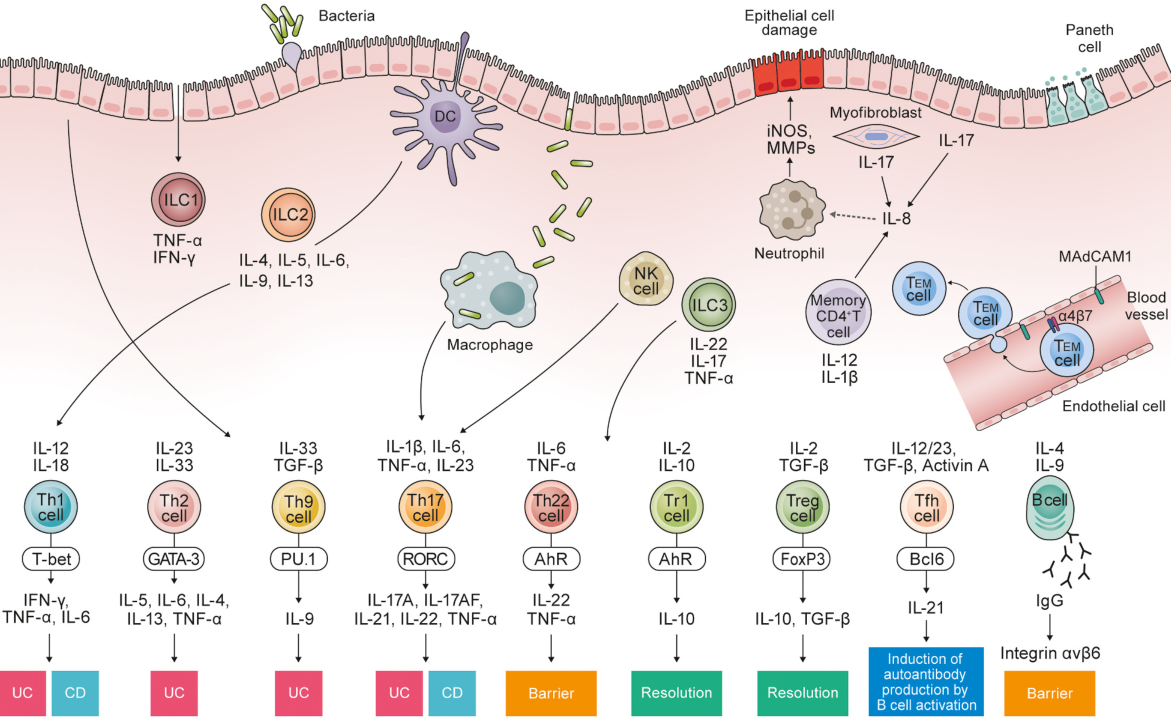
图4 免疫系统在UC发病机制中的调控作用[7]
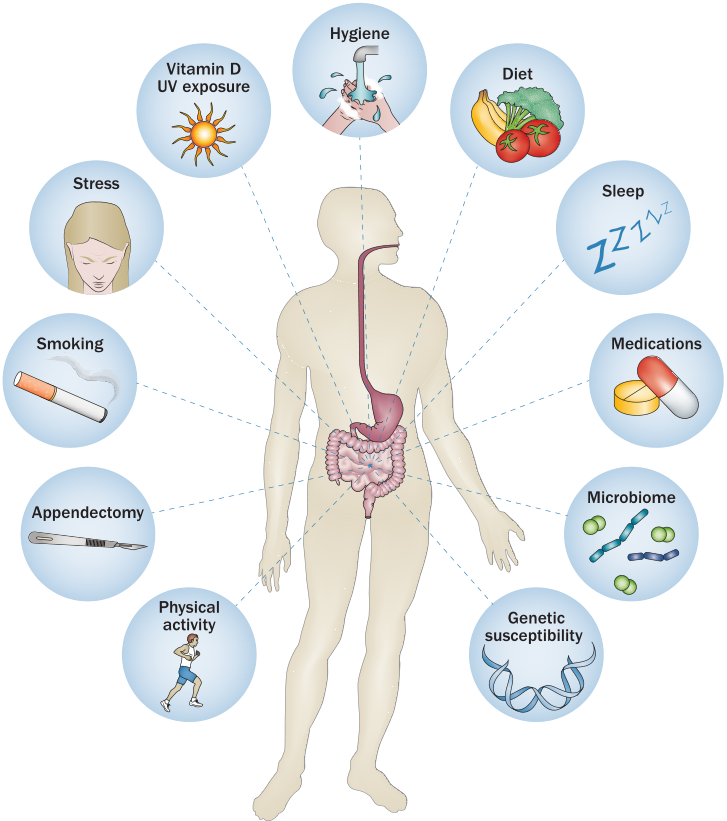
图5 影响UC发病的主要环境因素[8]
1.陌生的消化道疑难杂症——IBD
每年5月19日,紫色的灯光会照耀在世界各地的建筑上,人们使用“紫丝带”呼吁全世界关注并重视一种消化道难治病——炎症性肠病(Inflammatory Bowel Disease, IBD)。IBD是一种新兴疾病,最初于19世纪工业革命时期在西方国家被报道[1]。随着人类社会工业化和生活方式西式化的转变,IBD的发病率逐年上升,到目前全球已有超过1000万人罹患此病。IBD好发于欧美等发达国家,在美国的发病率已经超过0.3%[2]。尽管中国的发病率低于欧美等国,庞大的人口基数和快速的城市化进程仍使得中国的IBD病人数量快速增长且不容忽视。

图1 在世界IBD日被紫色灯光照射的世界各地

图2 世界IBD日的“紫丝带”标志
直到现在,人们对IBD的认知仍十分有限。IBD是一类病因尚不明确的慢性、特发性消化道疑难杂症,主要包括溃疡性结肠炎(Ulcerative Colitis, UC)和克罗恩病(Crohn’s Disease, CD)两种疾病表型。IBD具有无法治愈、病程反复、治疗困难、好发于青壮年的特点[3]。临床上,IBD病人普遍存在腹痛、腹泻、低烧、营养不良等症状。其中,UC病人会普遍出现脓血便和局限于结肠黏膜上层的炎症、溃疡等症状[4];而CD病人可在整个消化道范围内出现慢性炎症反应,表现出肠腔狭窄、瘘管、肠梗阻等疾病表现。此外,如果IBD病人不能实现有效的疾病控制,肠道癌变的风险将随着患病年限的推移而快速上升,最终将诱发小肠和结肠癌变[5]。

图3 UC和CD的肠道表现
2.尚未明确的致病机制——免疫、遗传、环境、微生物
目前,针对IBD的致病机制仍然没有统一的结论。免疫、遗传、环境、微生物被普遍认为是诱发IBD发病的四大因素。在基因层面,目前已经发现约250个基因位点与IBD有关,包括与上皮屏障、免疫反应、细胞自噬、细胞凋亡、氧化应激相关的基因[6]。这说明在IBD发病机制中存在基因与免疫系统以及肠道上皮之间的复杂关联。
在免疫层面,IBD的慢性炎症反应与免疫系统的调节失衡和过度激活存在直接联系(图4)。一般认为,免疫系统的激活起始于结肠上皮的破损和外界抗原的入侵,最初会引起固有免疫的激活,树突细胞、巨噬细胞、嗜中性粒细胞等会参与到这个过程中。而随着免疫系统和消化道炎症的反复激活,最终将逐渐形成不可逆的慢性炎症,这主要与适应免疫的激活有关。其中,Th1和Th17细胞及其相关炎性因子的激活被认为与CD发病有关;而Th2和Th17细胞及其相关炎性因子的激活被认为与UC发病有关。此外,调节T细胞、固有淋巴细胞、B细胞等也参与到了IBD的免疫进程中[7]。

图4 免疫系统在UC发病机制中的调控作用[7]
在环境层面,众多环境因素都与IBD的发病存在直接或间接的联系(图5)。城市化因素、空气污染、抗生素摄入、吸烟、消化道感染、日常饮食结构、精神压力等因素都会影响IBD的发病概率[8]。

图5 影响UC发病的主要环境因素[8]
在微生物层面,肠道菌群是维护结肠上皮微环境稳态的重要因素。目前已有大量文献表明肠道菌群的紊乱会加速IBD的疾病进展。IBD病人的肠道菌群紊乱是肠道上皮微环境恶化的表现,主要表现在菌群多样性的下降、菌群结构性的改变和潜在致病菌含量的升高[9]。肠道菌群和宿主的互作也是导致IBD疾病进展的重要因素。
综上所述,影响IBD发病的多种作用因素之间存在密切的相互关联。而这种复杂的多维度相互作用,最终形成了一个系统的IBD作用机制网络,这也给IBD发病机制的研究和临床治疗带来了巨大挑战。
综上所述,影响IBD发病的多种作用因素之间存在密切的相互关联。而这种复杂的多维度相互作用,最终形成了一个系统的IBD作用机制网络,这也给IBD发病机制的研究和临床治疗带来了巨大挑战。
4.复杂的药物疗法与无奈的手术疗法
复杂的发病因素和未知的致病机制很大程度上限制了IBD的治疗。临床上针对IBD的治疗主要分为药物疗法和手术疗法两类。在药物疗法中,对过度激活的免疫系统和炎症的抑制是药物的主要作用靶点。非甾体类抗炎药物(美沙拉嗪、奥沙拉嗪)、皮质类固醇(强的松、布地奈德)、免疫抑制剂(环孢素、甲氨蝶呤)、生物制剂(英夫利昔单抗、阿达木单抗)等都被广泛的应用于IBD的疾病治疗中[10]。需要指出的是,目前还没有任何一款针对IBD治疗的药物,IBD的药物疗法普遍存在用药流程复杂、用药种类多等弊端。同时,上述治疗药物多为广谱类药物,多存在明显的副作用,患者对药物的耐受性较差。这也导致在全世界每年有约15%的IBD病人因为“无药可治”而被迫接受手术治疗,这意味着病人消化道的切除和生活质量的严重下降[11]。因此,复杂且治疗效果有限的治疗方案往往给IBD病人带来了严重的生理负担和心理负担。
4.IBD的未来:新疗法、新药物
尽管自工业革命第一例IBD病例报道至今已有200余年的历史,人类对IBD的认知仍然十分有限。IBD作为一种极度复杂的消化道疾病,不仅仅是单纯的炎症性疾病。学界应当从更为全面的角度理解IBD的发病过程,将微生物、干细胞、环境等因素作为IBD治疗的潜在方向和靶标。目前,在学界已经提出了粪菌移植、干细胞疗法和饮食调控等新兴的治疗手段[12]。其中,粪菌移植已经应用在临床上并取得了积极的进展。从更为全面和更新的角度进行IBD的新药研发和新疗法研发可能是推动IBD疾病研究的重要思路和可行方案。
参考文献
[1]. Kaplan, G.G. and J.W. Windsor, The four epidemiological stages in the global evolution of inflammatory bowel disease. Nature reviews. Gastroenterology & hepatology, 2021. 18(1): p. 56-66.
[2]. Alatab, S., et al., The global, regional, and national burden of inflammatory bowel disease in 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. The Lancet Gastroenterology & Hepatology, 2020. 5(1): p. 17-30.
[3]. Kaplan, G.G. and S.C. Ng, Understanding and Preventing the Global Increase of Inflammatory Bowel Disease. Gastroenterology, 2017. 152(2): p. 313-321.e2.
[4]. Ungaro, R., et al., Ulcerative colitis. Lancet, 2017. 389: p. 1756-1770.
[5]. Torres, J., et al., Crohn's disease. The Lancet, 2017. 389: p. 1741-1755.
[6]. Khor, B., A. Gardet and R.J. Xavier, Genetics and pathogenesis of inflammatory bowel disease. Nature, 2011. 474(7351): p. 307-317.
[7]. Nakase, H., et al., The influence of cytokines on the complex pathology of ulcerative colitis. Autoimmunity Reviews, 2022. 21(3): p. 103017.
[8]. Ananthakrishnan, A.N., Epidemiology and risk factors for IBD. NATURE REVIEWS GASTROENTEROLOGY & HEPATOLOGY, 2015. 12(4): p. 205-217.
[9]. Imhann, F., et al., Interplay of host genetics and gut microbiota underlying the onset and clinical presentation of inflammatory bowel disease. Gut, 2017. 67(1): p. 108-119.
[10]. Nakase, H., et al., Evidence-based clinical practice guidelines for inflammatory bowel disease 2020. Journal of Gastroenterology, 2021. 56(6): p. 489-526.
[11]. Le Berre, C., et al., Ulcerative Colitis and Crohn's Disease Have Similar Burden and Goals for Treatment. Clinical Gastroenterology and Hepatology, 2020. 18(1): p. 14-23.
[12]. Ng, S.C. and A.N. Ananthakrishnan, New approaches along the IBD course: diet, tight control and stem cells. Nat Rev Gastroenterol Hepatol, 2019. 16(2): p. 82-84.
[1]. Kaplan, G.G. and J.W. Windsor, The four epidemiological stages in the global evolution of inflammatory bowel disease. Nature reviews. Gastroenterology & hepatology, 2021. 18(1): p. 56-66.
[2]. Alatab, S., et al., The global, regional, and national burden of inflammatory bowel disease in 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. The Lancet Gastroenterology & Hepatology, 2020. 5(1): p. 17-30.
[3]. Kaplan, G.G. and S.C. Ng, Understanding and Preventing the Global Increase of Inflammatory Bowel Disease. Gastroenterology, 2017. 152(2): p. 313-321.e2.
[4]. Ungaro, R., et al., Ulcerative colitis. Lancet, 2017. 389: p. 1756-1770.
[5]. Torres, J., et al., Crohn's disease. The Lancet, 2017. 389: p. 1741-1755.
[6]. Khor, B., A. Gardet and R.J. Xavier, Genetics and pathogenesis of inflammatory bowel disease. Nature, 2011. 474(7351): p. 307-317.
[7]. Nakase, H., et al., The influence of cytokines on the complex pathology of ulcerative colitis. Autoimmunity Reviews, 2022. 21(3): p. 103017.
[8]. Ananthakrishnan, A.N., Epidemiology and risk factors for IBD. NATURE REVIEWS GASTROENTEROLOGY & HEPATOLOGY, 2015. 12(4): p. 205-217.
[9]. Imhann, F., et al., Interplay of host genetics and gut microbiota underlying the onset and clinical presentation of inflammatory bowel disease. Gut, 2017. 67(1): p. 108-119.
[10]. Nakase, H., et al., Evidence-based clinical practice guidelines for inflammatory bowel disease 2020. Journal of Gastroenterology, 2021. 56(6): p. 489-526.
[11]. Le Berre, C., et al., Ulcerative Colitis and Crohn's Disease Have Similar Burden and Goals for Treatment. Clinical Gastroenterology and Hepatology, 2020. 18(1): p. 14-23.
[12]. Ng, S.C. and A.N. Ananthakrishnan, New approaches along the IBD course: diet, tight control and stem cells. Nat Rev Gastroenterol Hepatol, 2019. 16(2): p. 82-84.






