江苏集萃药康生物科技股份有限公司品牌商
7 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
斑点鼠(基因编辑KO/CKO小鼠)
¥10000 - 20000
品牌商
江苏集萃药康生物科技股份有限公司
入驻年限:7 年
- 联系人:
药康生物
- 所在地区:
江苏 南京市 浦口区
- 业务范围:
抗体、细胞库 / 细胞培养、技术服务、试剂、耗材、实验室仪器 / 设备
- 经营模式:
生产厂商 代理商 科研机构
公司新闻/正文
斑点鼠助力脓毒症机理研究与相关治疗药物开发
1005 人阅读发布时间:2022-03-11 17:48

肝素是一种具有抗凝作用的哺乳动物多糖,已被广泛用于治疗各种血栓性疾病,如静脉血栓栓塞。除血栓性疾病外,相关研究和临床实践证据表明,肝素治疗可改善败血症症状(一种感染诱导的伴有器官功能障碍的危重症)。尽管肝素如何发挥其抗凝作用已相对比较清楚,但肝素所能实现的免疫调节机制仍然是个谜。
2021 年 2 月 8 日,中南大学吕奔团队在 Immunity 在线发表题为「Heparin prevents caspase- 11 -dependent septic lethality independent of anticoagulant properties」的研究论文,该研究使用了集萃药康斑点鼠(B6 /JGpt-Hpseem1Cd1095/Gpt, T017525),报道了肝素可预防败血症中 caspase- 11 依赖性免疫反应和致死性,而与其抗凝特性无关。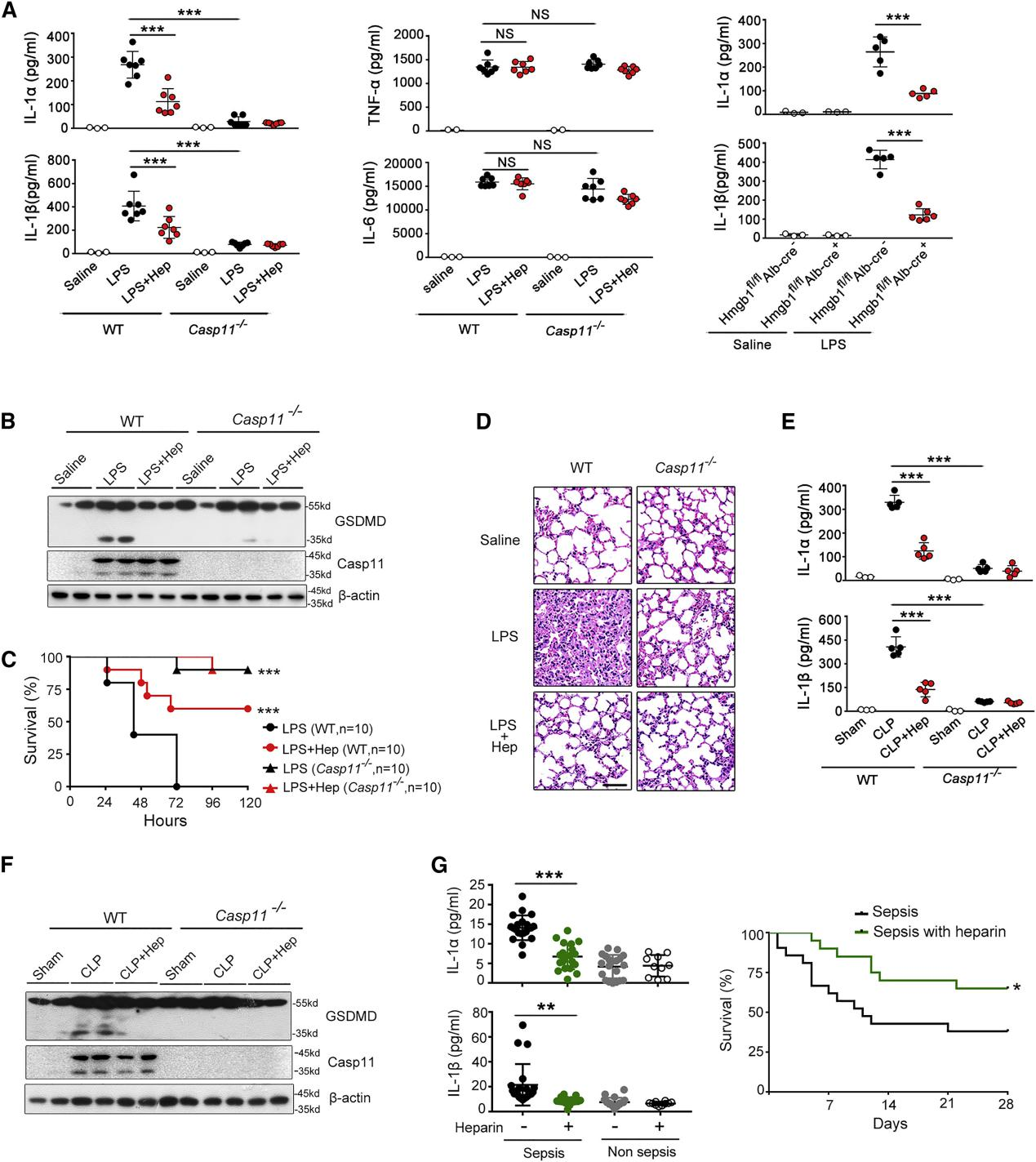
图 1. 肝素阻止败血症中 caspase- 11 依赖的免疫反应和致死性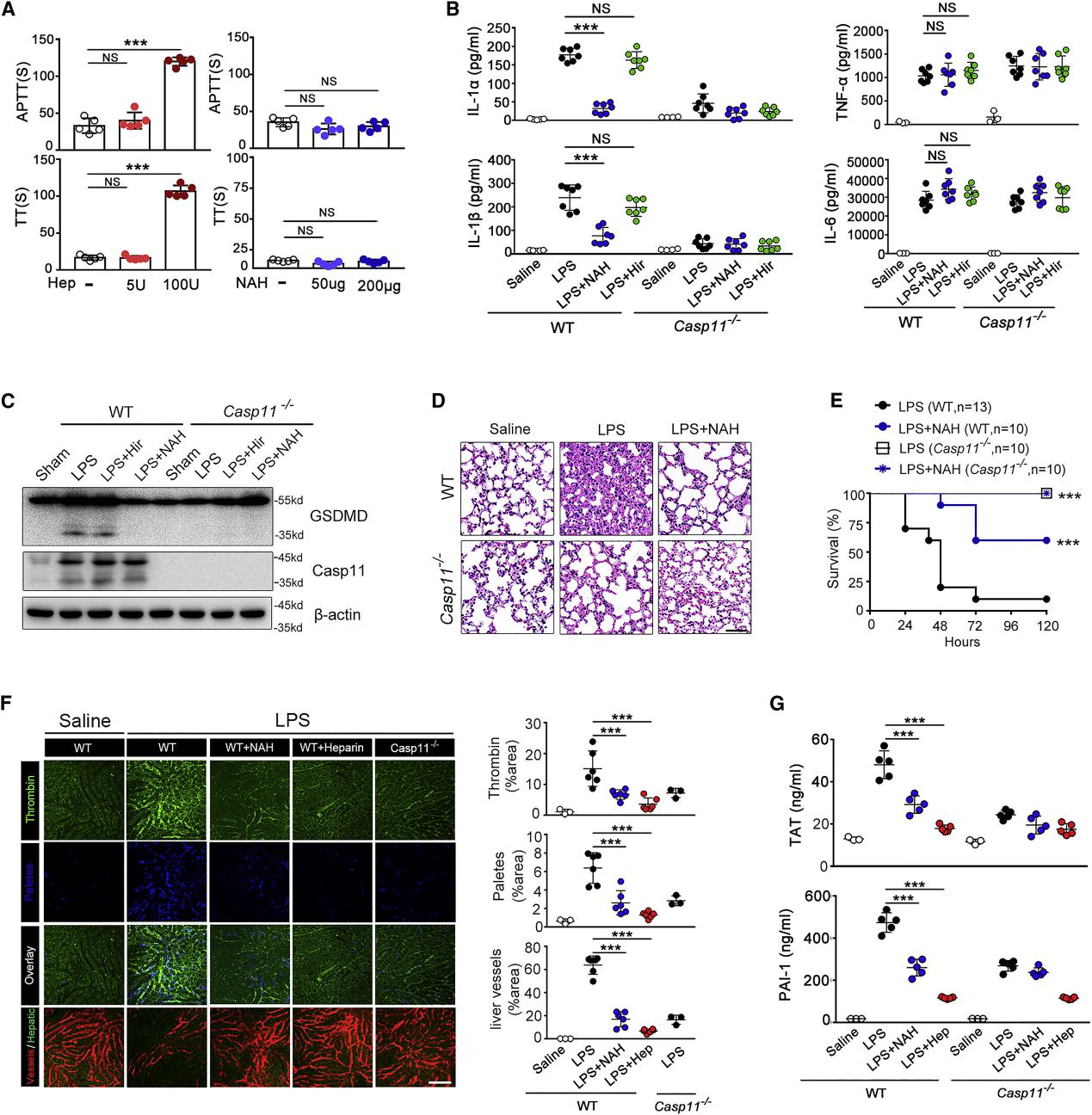
图 2. 肝素抑制 caspase- 11 活化与其抗凝特性无关
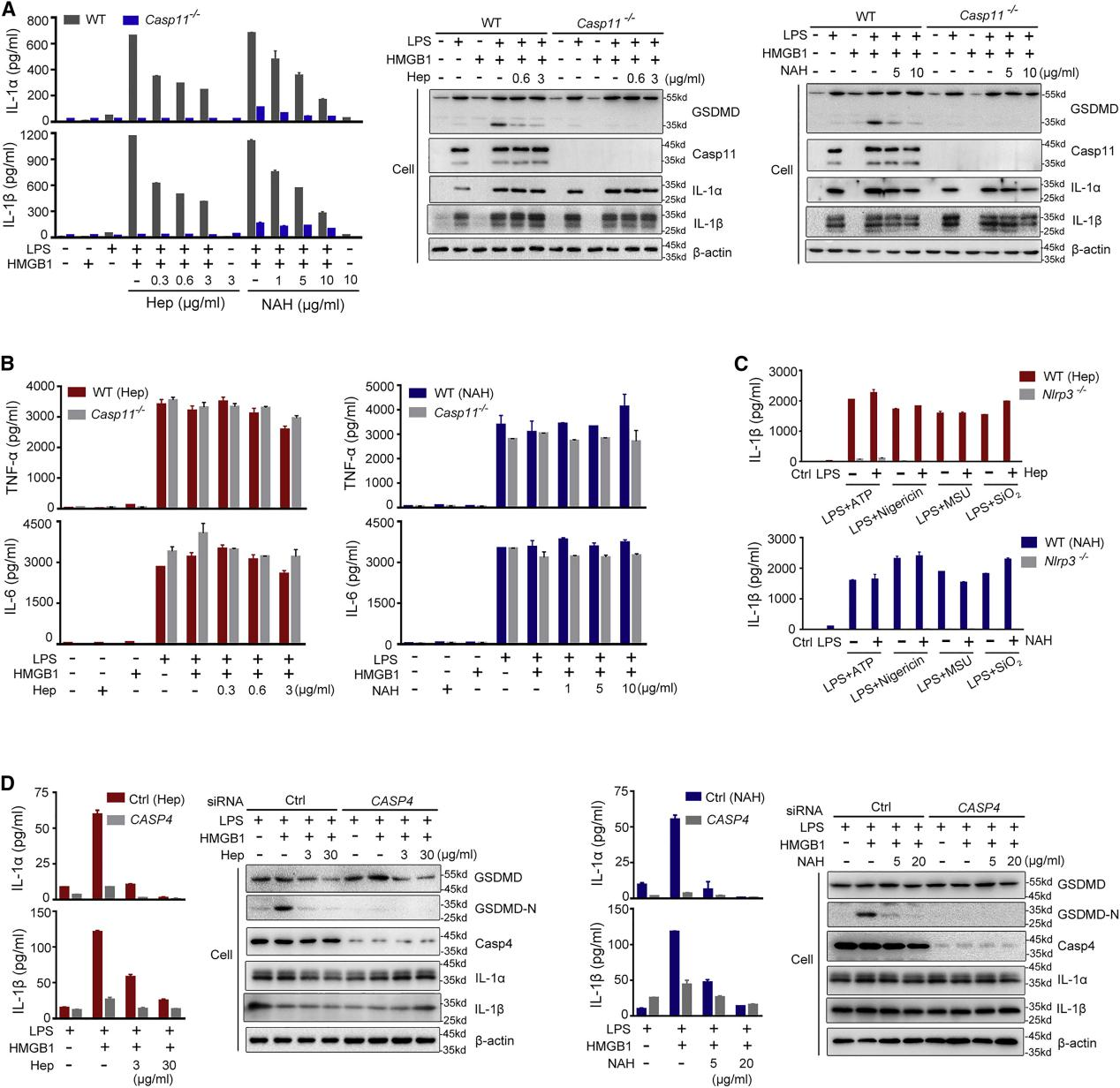
图 3. 肝素在体外选择性抑制重组 HMGB1 和 caspase- 11 依赖性免疫应答
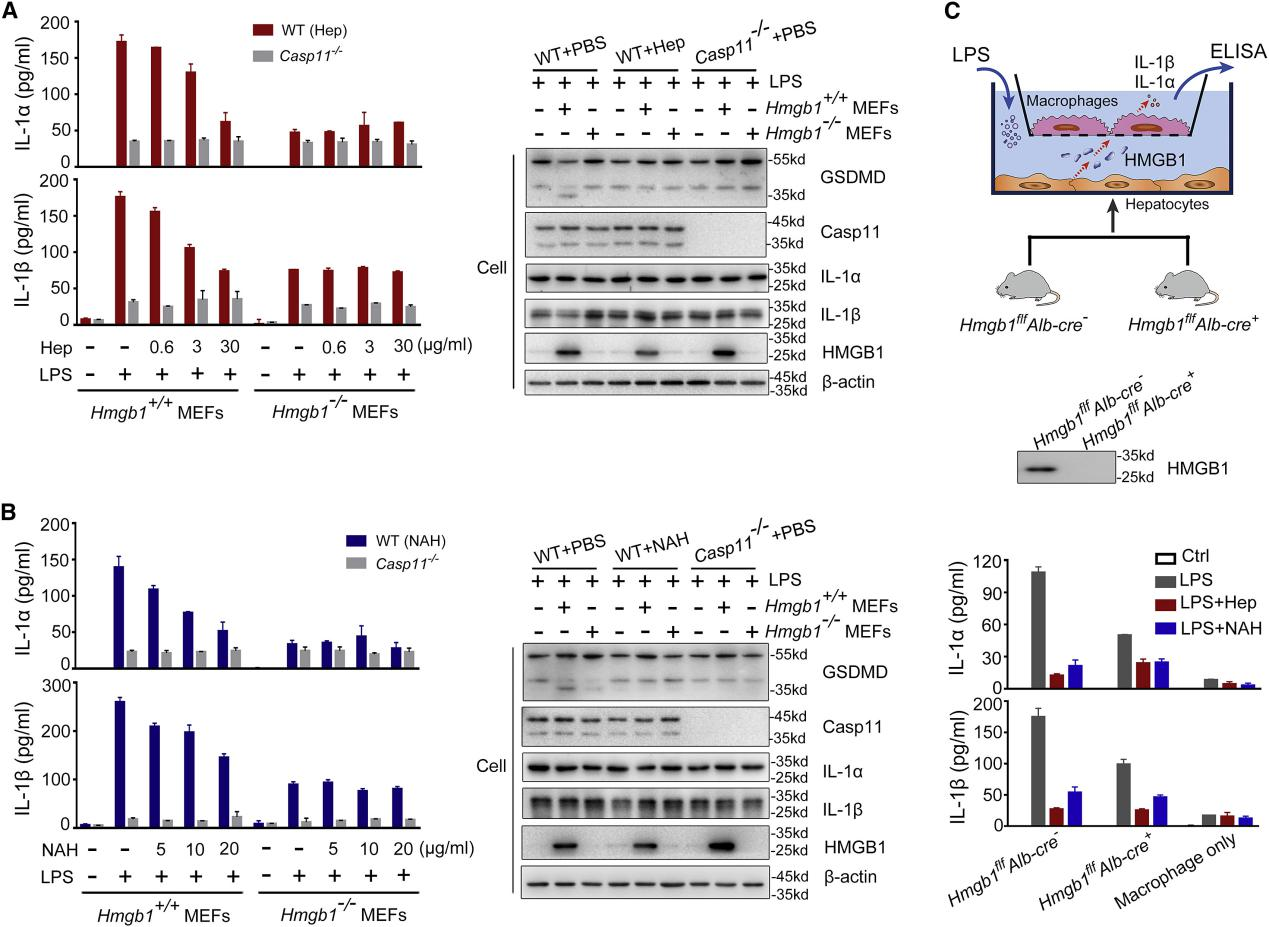
图 4. 肝素在体外抑制内源性 HMGB1 和 caspase- 11 依赖性免疫应答
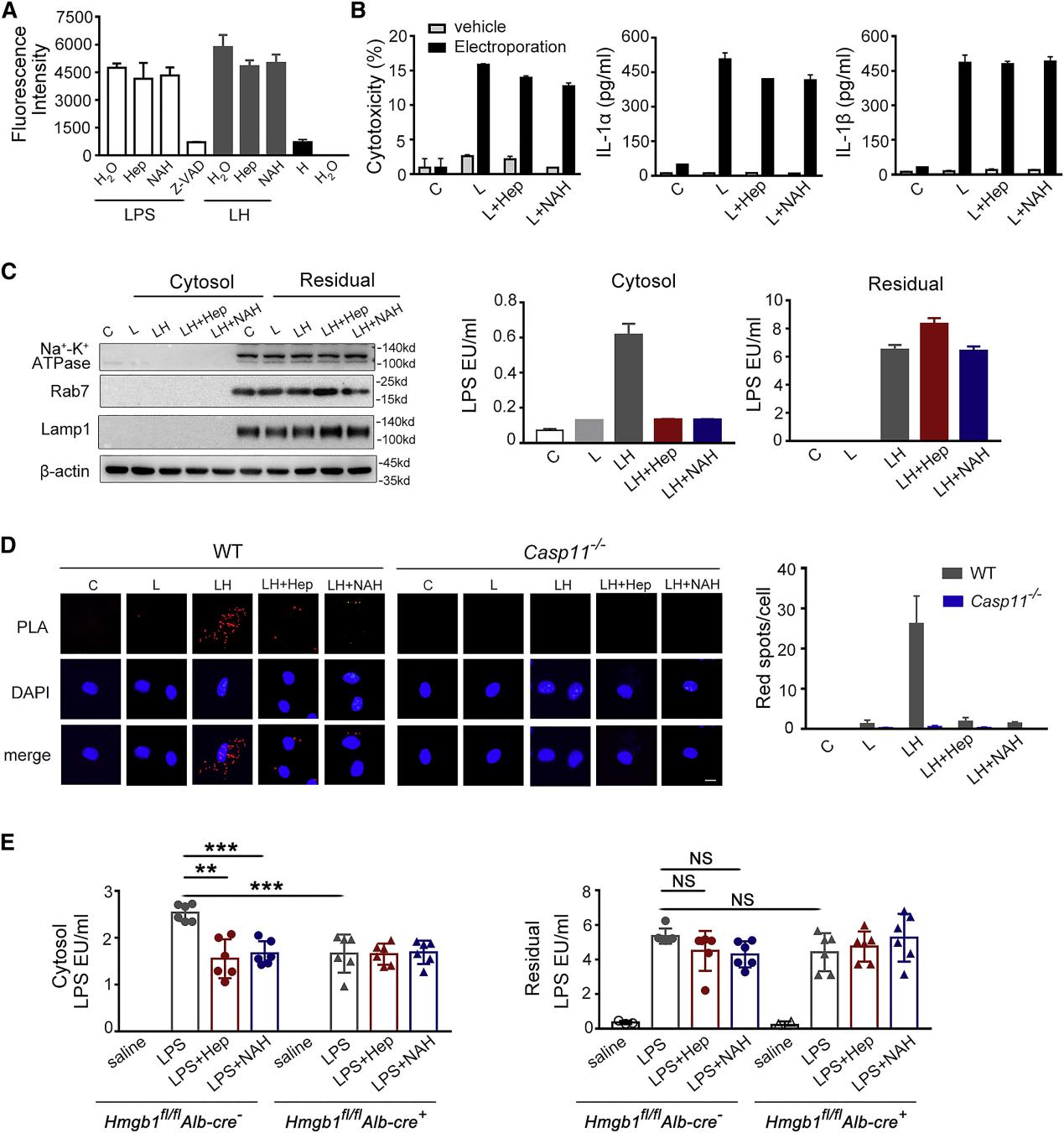
图 5. 肝素通过抑制 HMGB1 介导的 LPS 胞质转运来抑制caspase- 11 活化
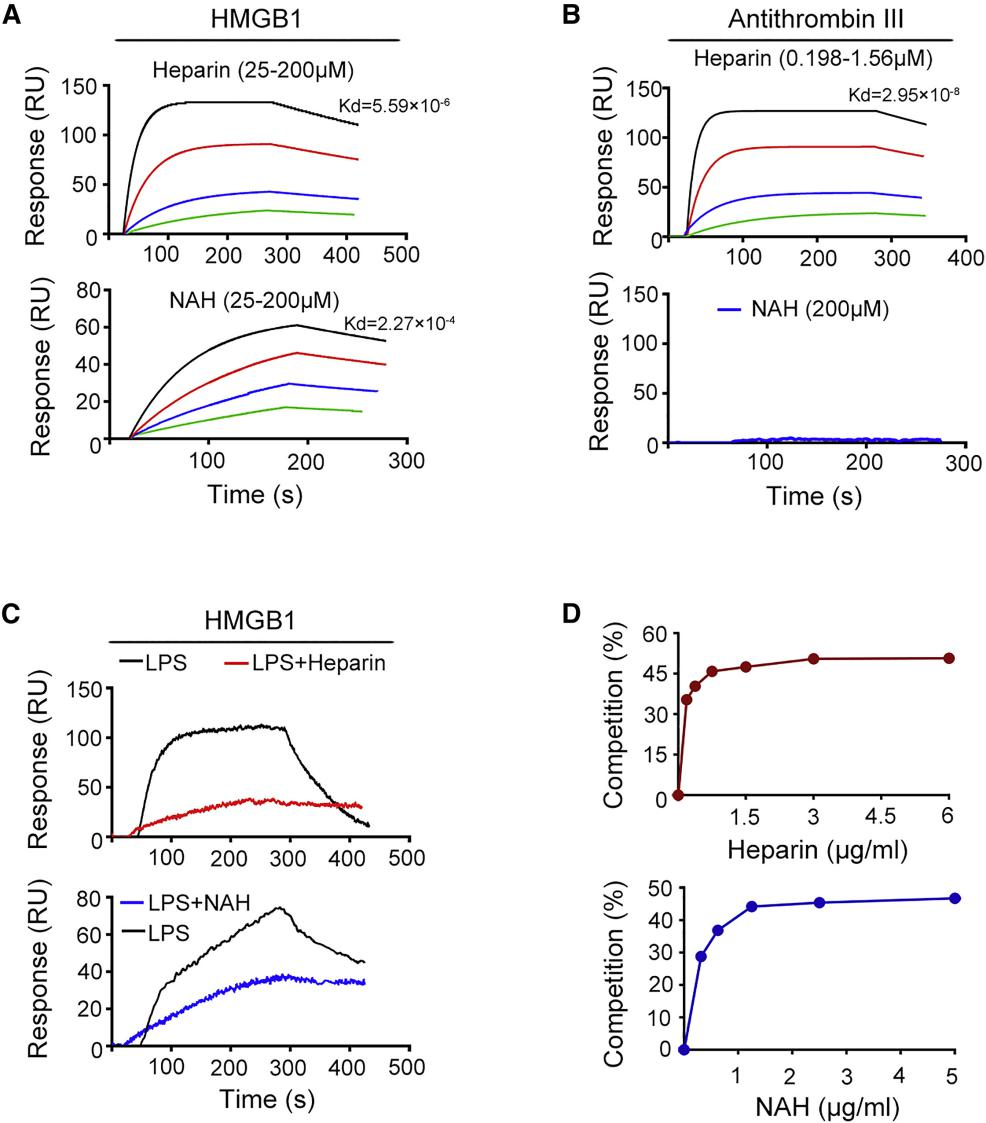
图 6. 肝素抑制 HMGB1 -LPS 结合
2021 年 2 月 8 日,中南大学吕奔团队在 Immunity 在线发表题为「Heparin prevents caspase- 11 -dependent septic lethality independent of anticoagulant properties」的研究论文,该研究使用了集萃药康斑点鼠(B6 /JGpt-Hpseem1Cd1095/Gpt, T017525),报道了肝素可预防败血症中 caspase- 11 依赖性免疫反应和致死性,而与其抗凝特性无关。
-
肝素阻止败血症中 caspase- 11 依赖性免疫反应和致死性

图 1. 肝素阻止败血症中 caspase- 11 依赖的免疫反应和致死性
2. 肝素抑制 caspase- 11 活化与其抗凝特性无关
研究者通过使用硫酸化肝素(NAH)(硫酸化肝素是一种化学修饰的肝素,不会发挥抗凝特性)来给药。发现硫酸化非抗凝肝素 (NAH) 剂量依赖性地阻断内毒素血症中的 caspase- 11 介导的免疫反应和动物致死性,而不影响 TNF 或 IL- 6 的血浆浓度;NAH 处理显著降低了 LPS 激发后的凝血酶活化,其方式与 caspase- 11 缺陷相似;NAH 治疗阻止 LPS 诱导的血浆 TAT 复合物、D-二聚体和 PAI- 1 的增加,其方式与 caspase- 11 缺陷相似(图 2)。

图 2. 肝素抑制 caspase- 11 活化与其抗凝特性无关
3. 肝素在体外选择性抑制 HMGB1 和 caspase- 11 依赖性免疫应答
研究者先用重组 HMGB1 蛋白与 LPS 诱导,发现WT 而不是 caspase- 11 缺陷的腹腔小鼠巨噬细胞释放 IL- 1a、IL- 1b 和乳酸脱氢酶 (LDH) 以及 GSDMD 裂解且肝素呈剂量依赖性抑制 Caspase- 11 依赖性免疫应答和 GSDMD 裂解(图 3)。

图 3. 肝素在体外选择性抑制重组 HMGB1 和 caspase- 11 依赖性免疫应答
接着研究者用 LPS 和 HMGB1 +/+ 或 HMGB1 -/-小鼠胚胎成纤维细胞 (MEFs) 的坏死细胞裂解物刺激小鼠腹腔巨噬细胞,发现仅来源于 Hmgb1 +/+ MEFs 的坏死细胞裂解物使 LPS 能够以 caspase- 11 依赖性方式诱导 IL- 1a 和 IL- 1b 的强烈释放以及 GSDMD 裂解,此时加入肝素可以剂量依赖性地抑制 IL- 1a 和 IL- 1b 的释放,并阻断 GSDMD 的裂解。用HMGB1 +/+ 或 HMGB1 -/-小鼠肝细胞与小鼠腹腔巨噬细胞共培养,向细胞培养基中加入肝素可阻断 caspase- 11 依赖性免疫应答和 GSDMD 孔形成(图 4)。

图 4. 肝素在体外抑制内源性 HMGB1 和 caspase- 11 依赖性免疫应答
4. 肝素通过抑制 HMGB1 介导的 LPS 胞质转运抑制 caspase- 11 活化
研究者用 LPS 和 HMGB1 刺激巨噬细胞,发现加入肝素可显著降低巨噬细胞胞质中 LPS 的浓度;使用近端连接试验 (PLA)发现HMGB1 显著促进 LPS-caspase- 11 相互作用,加入肝素可减少胞质中 LPS-caspase- 11 相互作用;用肝细胞 HMGB1 缺陷小鼠及其对照小鼠进行致死性内毒素血症,伴或不伴肝素处理,发现肝素处理显著降低了对照小鼠而不是 HMGB1 缺陷小鼠脾细胞胞质中的 LPS 浓度(图 5)。

图 5. 肝素通过抑制 HMGB1 介导的 LPS 胞质转运来抑制caspase- 11 活化
5. 肝素直接抑制 HMGB1 -LPS 结合
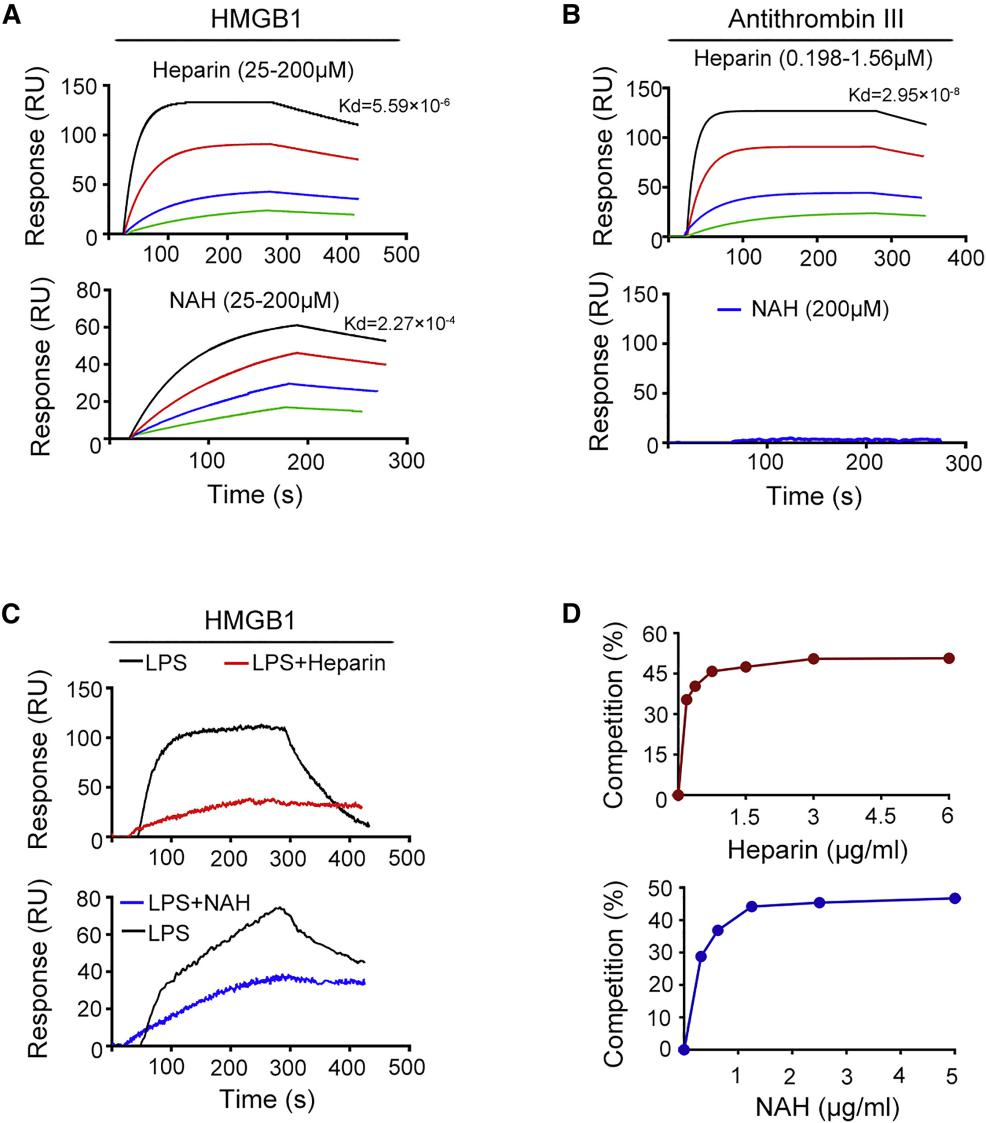
研究者通过表面等离子体共振 (SPR) 显示肝素和 NAH 均能够阻止 HMGB1 -LPS 结合;使用 PLA 定量测定了 HMGB1 + LPS- 刺激的巨噬细胞表面和内部的 HMGB1 -LPS 复合物,加入肝素可显著降低细胞表面或细胞内检测到的 HMGB1 -LPS 复合物数量(图 6)。

图 6. 肝素抑制 HMGB1 -LPS 结合
6. 肝素通过阻止乙酰肝素酶介导的糖萼降解抑制 LPS 的胞质转运
研究者使用OMV 刺激的小鼠巨噬细胞,加入肝素或 NAH 可显著减少该巨噬细胞 LPS 胞质转运;通过乙酰肝素酶的基因缺失或添加肝素或 NAH可阻止 HMGB1 + LPS 或 OMV 刺激导致的糖萼的密度降低。使用重组乙酰肝素酶人工降解巨噬细胞的糖萼,导致胞质中 LPS 浓度增加(图 7)。
图 7. 肝素通过阻止乙酰肝素酶介导的糖萼降解,抑制 LPS 的胞质转运
结论
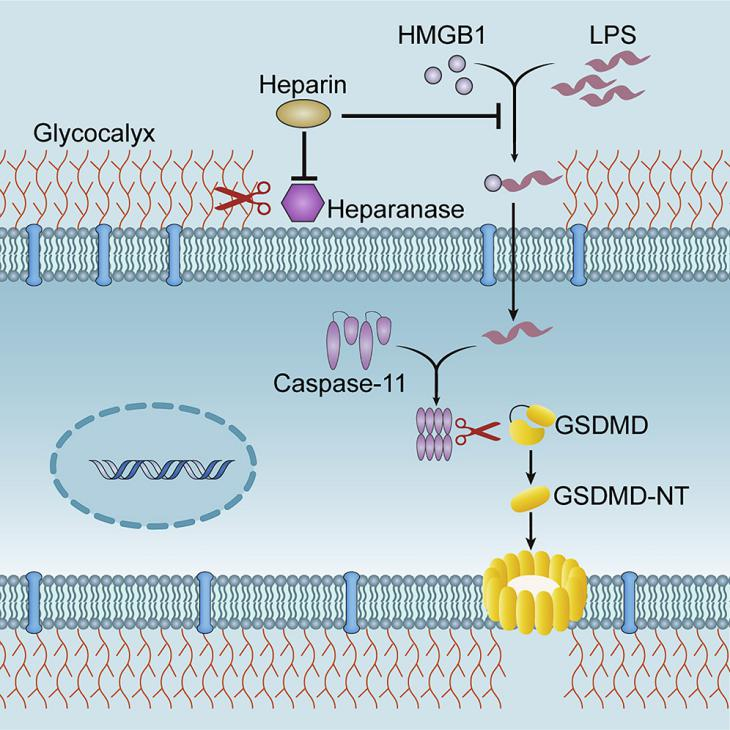

研究表明,肝素或无抗凝功能的硫酸化肝素 (NAH)抑制了 HMGB1与脂多糖(LPS)的结合,并可以阻止乙酰肝素酶降解巨噬细胞的糖萼,这些两个过程的发生阻止了 LPS 的胞质传递和 caspase- 11 的激活,进而阻止 GSDMD 的裂解成为 GSDMD-NT。
临床上接受肝素治疗的败血症患者的生存率高于未接受肝素治疗的败血症患者。然而,更广泛使用肝素治疗败血症的一个障碍是出血风险。无抗凝活性的改良肝素给药对凝血无影响。这种以前未被认识的肝素功能的鉴定确立了先天性免疫反应和凝血之间的联系。
集萃药康斑点鼠计划为该研究提供了相应的模型支持。集萃药康斑点鼠计划旨在对小鼠基因组中可设计策略的所有蛋白编码和非编码基因逐一进行 CKO/KO 模型制作,最终形成小鼠全部基因型品系库,实现快速供鼠。当前,斑点鼠总品系数量达 22000 +,覆盖肿瘤、代谢、免疫、发育、DNA 及蛋白修饰等诸多热门领域,满足不同方向科研人员实验用鼠需求。
临床上接受肝素治疗的败血症患者的生存率高于未接受肝素治疗的败血症患者。然而,更广泛使用肝素治疗败血症的一个障碍是出血风险。无抗凝活性的改良肝素给药对凝血无影响。这种以前未被认识的肝素功能的鉴定确立了先天性免疫反应和凝血之间的联系。
集萃药康斑点鼠计划为该研究提供了相应的模型支持。集萃药康斑点鼠计划旨在对小鼠基因组中可设计策略的所有蛋白编码和非编码基因逐一进行 CKO/KO 模型制作,最终形成小鼠全部基因型品系库,实现快速供鼠。当前,斑点鼠总品系数量达 22000 +,覆盖肿瘤、代谢、免疫、发育、DNA 及蛋白修饰等诸多热门领域,满足不同方向科研人员实验用鼠需求。






